基因治療涉及到將外源基因導入細胞內使其能夠表達特定產物或調節、抑制某個生物學功能。然而,基因遞送受到許多細胞外和細胞內屏障的阻礙,因此需要合適的載體來提高遞送效率。基于多肽的基因遞送系統已成為一類新的非病毒載體,與聚合物和脂質載體相比,具有較好的生物相容性、設計多樣性、易于合成和免疫反應風險較低等優點。然而,多肽遞送體系目前還不成熟,需要進一步梳理和優化設計以提高其遞送效率和細胞靶向性。近期,我校藥學院招秀伯團隊發表綜述論文,回顧了常見基因遞送方法及其優缺點;概述了幾種常見被遞送核酸(如質粒DNA、反義寡核苷酸、mRNA、siRNA等)的工作原理;介紹了基于多肽的基因遞送系統的最新研究進展;分別討論了陽離子兩親性肽(CAPs)、細胞穿膜肽(CPPs)和肽基兩親性分子(PAs)等3種不同類型的多肽體系的結構特征及其在基因遞送方面的應用,從化學結構的角度對不同類別多肽的遞送效率及其靶向基因遞送能力進行了比較,為新型、高效、組織特異性基因遞送的多肽載體的合理設計提供指導。
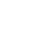
圖1. 多肽遞送質粒DNA(pDNA)、mRNA、siRNA的示意圖。多肽先與核酸通過靜電作用形成納米顆粒復合體,通過內吞作用將其轉運到細胞內,再從內涵體逃逸,將核酸釋放到細胞質或細胞核內。

圖2. mRNA, siRNA, 反義寡核苷酸的細胞內通路示意圖。
該綜述近期發表在藥物遞送領域的top期刊《控制釋放雜志》(SCI一區Top,影響因子9.8 ),論文題目為”多肽用于基因遞送的最新進展”,并被《控制釋放雜志》微信公眾號報道(https://mp.weixin.qq.com/s/pbn3BoAp4BnT5RiedG_Bhg)。該綜述與英國謝菲爾德大學合作,第一作者為謝菲爾德大學Roja Hadianamrei博士,招秀伯教授為本文通訊作者。
據悉,招秀伯團隊近兩年在多肽的抗腫瘤、基因遞送及組織工程等領域的應用方面取得了諸多成果。相關論文發表在《國際制藥學雜志》2022, 617, 121619.;《膠體與界面科學雜志》2022, 607, 488-501.;《膠體與表面,B 輯:生物界面》2022, 209, 112165.;《美國化學學會應用材料與界面》2021, 13, 49713–49728.;《膠體與界面科學雜志》2021, 603, 380-390.;《自然科學進展?國際材料》 2020, 30, 686–696.等期刊上。(通訊員/王憶波 審核/張繼延 張屹 編輯/孫悅)
文章鏈接:https://doi.org/10.1016/j.jconrel.2022.02.010